| 前沿探索 | 我校科研团队在多模态肿瘤协同治疗领域取得新突破 |
| 发布人:曾铮 发布时间:2026-03-23 浏览次数:10 |
|
近日,生物与医学工程学院权静副教授团队联合上海交通大学医学院附属同仁医院孙鹏主任团队,以“基于CaO₂的AuPt双金属纳米酶级联催化用于协同化学动力学/光热/免疫治疗”(CaO₂-based AuPt Bimetallic Nanozymes with Cascade Catalysis for Synergistic Chemodynamic/Photothermal/Immunotherapy)为题,在《化学工程杂志》(Chemical Engineering Journal)上发表研究成果,为肿瘤治疗提供全新方案。
基于纳米酶的化学动力学治疗(CDT),凭借安全性高、无需外源供氧、可调控肿瘤微环境等优势,近年来成为肿瘤治疗领域的研究热点。该疗法依托Fenton/类Fenton反应,将肿瘤内源性H₂O₂转化为高毒性ROS杀伤肿瘤细胞,但临床转化面临两大核心瓶颈:一是纳米酶催化活性不足,二是肿瘤微环境H₂O₂浓度极低(仅50-100×10⁻⁶ M),难以生成足量ROS。此外,单一治疗模式无法彻底清除肿瘤、遏制复发转移,严重限制临床应用。因此,构建高效自供H₂O₂纳米酶体系、整合多模式协同治疗,成为肿瘤纳米医学领域的关键研究方向。针对上述难题,科研团队依托医工交叉开展攻关,研发出基于过氧化钙(CaO₂)的AuPt双金属自级联纳米酶体系CaO₂/AuPt@BSA(CAPB),实现化学动力学、光热、免疫三重协同抗肿瘤治疗。论文通讯作者为权静、孙鹏,共同第一作者包括生物与医学工程学院研究生刘文涛、朱丽丽。
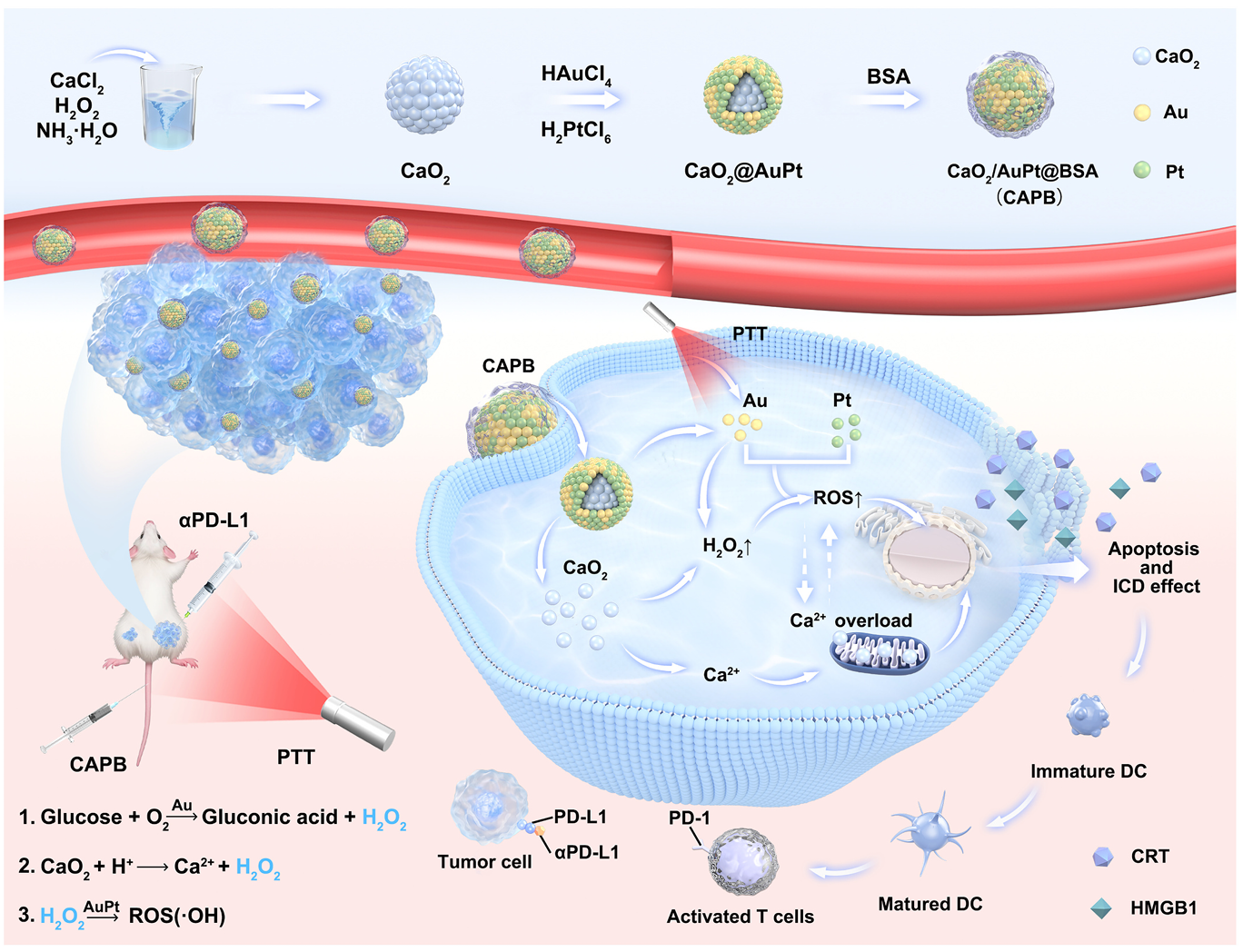
(方案1(a)CAPB纳米酶制备的示意图;(b)肿瘤治疗的作用机制。) 该CAPB纳米酶体系根据肿瘤微环境的酸性及代谢特征设计,采用氯化钙法构建具有良好生物相容性的CaO₂纳米球核心,并集成Au与Pt双金属纳米酶,通过BSA表面包封实现了优异的肿瘤靶向性与物理稳定性(平均粒径约200 nm且在7天内保持稳定)。该体系通过高效的自级联催化反应精准打击肿瘤:进入酸性肿瘤微环境后,Au纳米酶通过消耗葡萄糖实现“饥饿疗法”并产生H₂O₂,随后Pt纳米酶接力催化生成高毒性羟基自由基(•OH)以增强化学动力学治疗(CDT)疗效,同时CaO₂分解释放的Ca²⁺可诱导严重的线粒体功能障碍。 在能量转换与催化性能方面,Au纳米酶还赋予了该体系优异的光热转换效能(效率达36.3%),在808 nm激光照射下能使环境温度显著升高(400 μg/mL溶液升温约38°C),不仅能实现肿瘤的光热消融(PTT),更能显著加速级联催化反应动力学(Km为39.178 ± 7.656 mM,Vmax = 2.249×10⁻⁶ ± 1.923×10⁻⁷ M min⁻¹)。体外实验证实,该体系能精准识别并杀伤4T1肿瘤细胞,其细胞凋亡率在光热增强下高达58.8%,且表现出较低的正常细胞毒性。 在体内抗肿瘤疗效及免疫激活方面,CAPB纳米酶展现出强大的协同治疗能力。动物实验显示,该纳米酶在给药8小时后富集于肿瘤部位,联合αPD-L1抗体治疗后实现了82.7%的原发肿瘤抑制率,原发抑瘤率达到单独免疫治疗组的1.67倍,且远端肿瘤抑制率亦高达79.18%。这种显著的疗效归因于CDT与PTT协同诱导的免疫原性细胞死亡(ICD),其有效促进了损伤相关分子模式(DAMPs)的释放,使体内成熟树突状细胞(DCs)和CD8⁺ T细胞比例分别提升至对照组的2.60倍和1.73倍,并上调了TNF-α和IL-12等关键免疫因子水平。这一种结合催化、光热与免疫的三重协同策略,在显著抑制肿瘤生长与转移的同时展现了良好的生物安全性,为多模态肿瘤协同治疗提供了强有力的科学依据与应用前景。 本研究得到“上海市同仁医院-东华大学医工交叉项目”等多项科研资助,体现了校院深度合作在推动医学科技创新、助力区域高质量发展中的重要实践与价值。 原文链接:https://doi.org/10.1016/j.cej.2026.17256 |